ਸੰਯੋਜਕਤਾ
ਸੰਯੋਜਕਤਾ ਕਿਸੇ ਪਰਮਾਣੂ ਦੇ ਸਭ ਤੋਂ ਬਾਹਰਲੇ ਸ਼ੈੱਲ ਵਿੱਚ ਮੌਜੂਦ ਇਲੈਕਟ੍ਰਾੱਨਾ ਨੂੰ ਸੰਯੋਜਕਤਾ-ਇਲੈਕਟ੍ਰਾੱਨ ਕਹਿੰਦੇ ਹਨ। ਨੀਲ ਬੋਹਰ-ਬਰੀ ਸਕੀਮ ਅਨੁਸਾਰ ਕਿਸੇ ਵੀ ਪਰਮਾਣੂ ਦਾ ਸਭ ਤੋਂ ਬਾਹਰੀ ਸ਼ੈਲ ਵੱਧ ਤੋਂ ਵੱਧ 8 ਇਲੈਕਟ੍ਰਾਨ ਰੱਖ ਸਕਦਾ ਹੈ। ਜਿਹਨਾਂ ਪਰਮਾਣੂਆਂ ਦੇ ਸਭ ਤੋਂ ਬਾਹਰੀ ਸ਼ੈਲ ਪੂਰਣ ਰੂਪ ਵਿੱਚ ਭਰੇ ਹੁੰਦੇ ਹਨ, ਉਹ ਰਸਾਇਣਿਕ ਰੂਪ ਵਿੱਚ ਕਿਰਿਆਸ਼ੀਲ ਨਹੀਂ ਹੁੰਦੇ ਅਤੇ ਉਨ੍ਹਾਂ ਦੀ ਸੰਯੋਜਕਤਾ ਸਿਫਰ ਹੁੰਦੀ ਹੈ। ਜਿਵੇਂ ਹੀਲੀਅਮ, ਆਰਗਨ ਆਦਿ। ਅੱਠ ਇਲੈਕਟ੍ਰਾਨ ਵਾਲੇ ਸਭ ਤੋਂ ਬਾਹਰੀ ਸ਼ੈਲ ਨੂੰ ਅਸ਼ਟਕ ਮੰਨਿਆ ਜਾਂਦਾ ਹੈ। ਪਰਮਾਣੂ ਆਪਣੇ ਅੰਤਿਮ ਸ਼ੈਲ ਵਿੱਚ ਅਸ਼ਟਕ ਪ੍ਰਾਪਤ ਕਰਨ ਲਈ ਕਿਰਿਆ ਕਰਦੇ ਹਨ। ਇਹ ਆਪਸ ਵਿੱਚ ਇਲੈਕਟ੍ਰਾਨਾਂ ਦੀ ਸਾਂਝੇਦਾਰੀ ਕਰਨ, ਇਨ੍ਹਾਂ ਨੂੰ ਗ੍ਰਹਿਣ ਕਰਨ ਜਾਂ ਤਿਆਗ ਕਰਨ ਨਾਲ ਹੁੰਦਾ ਹੈ। ਪਰਮਾਣੂ ਦੇ ਸਭ ਤੋਂ ਬਾਹਰੀ ਸ਼ੈਲ ਵਿੱਚ ਇਲੈਕਟ੍ਰਾਨਾਂ ਦੇ ਅਸ਼ਟਕ ਬਣਾਉਣ ਦੇ ਲਈ ਜਿੰਨੀ ਸੰਖਿਆ ਵਿੱਚ ਇਲੈਕਟ੍ਰਾਨਾਂ ਦੀ ਸਾਂਝੇਦਾਰੀ ਜਾਂ ਸਥਾਨ ਅੰਤਰਨ ਹੁੰਦਾ ਹੈ, ਉਹੀ ਉਸ ਤੱਤ ਦੀ ਸੰਯੋਜਕਤਾ ਸ਼ਕਤੀ ਜਾਂ ਸੰਯੋਜਕਤ ਹੁੰਦੀ ਹੈ।[1] ਹਾਈਡ੍ਰੋਜਨ ਅਤੇ ਹੀਲੀਅਮ ਹਰੇਕ ਦੇ ਪਰਮਾਣੂਆਂ ਦੇ ਸਭ ਤੋਂ ਬਾਹਰੀ ਸ਼ੈਲ ਵਿੱਚ ਇੱਕ-ਇੱਕ ਇਲੈਕਟ੍ਰਾਨ ਹੁੰਦਾ ਹੈ। ਇਸ ਲਈ ਇਨ੍ਹਾਂ ਦੀ ਸੰਯੋਜਕਤ ਇੱਕ ਕਹੀ ਜਾਂਦੀ ਹੈ। ਮੈਗਨੀਸ਼ੀਅਮ ਦੀ ਦੋ ਸੰਯੋਜਕਤਾ ਅਤੇ ਐਲੁਮੀਨੀਅਮ ਦੀ ਸੰਯੋਜਕਤਾ ਤਿੰਨ ਹੁੰਦੀ ਹੈ। ਫਲੋਰੀਨ, ਕਲੋਰੀਨ ਦੇ ਸਭ ਤੋਂ ਬਾਹਰੀ ਸ਼ੈਲ ਵਿੱਚ ਸੱਤ ਇਲੈਕਟ੍ਰਾਨ ਹੁੰਦੇ ਹਨ ਇਸ ਬਾਹਰੀ ਸ਼ੈਲ ਵਿੱਚ ਅਸ਼ਟਕ ਬਣਾਉਣ ਲਈ ਇਨ੍ਹਾਂ ਨੂੰ ਸੱਤ ਇਲੈਕਟ੍ਰਾਨਾਂ ਦਾ ਤਿਆਗ ਕਰਨ ਦੀ ਬਜਾਏ ਇੱਕ ਇਲੈਕਟ੍ਰਾਨ ਪ੍ਰਾਪਤ ਕਰਨਾ ਵਧੇਰੇ ਸੌਖਾ ਹੈ ਇਸ ਲਈ ਇਨ੍ਹਾਂ ਦੀ ਸੰਯੋਜਕਤਾ ਅਸ਼ਟਕ ਵਿੱਚੋਂ ਸੱਤ ਘਟਾ ਕੇ ਪ੍ਰਾਪਤ ਕੀਤੀ ਜਾਂਦੀ ਹੈ ਇਸ ਲਈ ਫਲੋਰੀਨ ਅਤੇ ਕਲੋਰੀਨ ਦੀ ਸੰਯੋਜਕਤਾ ਇੱਕ ਹੈ। ਇਵੇ ਹੀ ਆਕਸੀਜਨ ਦੀ ਸੰਯੋਜਕਤਾ ਦੋ ਹੈ ਨਾਂ ਕਿ ਛੇ।
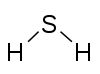
| ਯੋਗਿਕ | H2 | CH4 | C3H8 | C2H2 | NH3 | NaCN | H2S | H2SO4 | Cl2O7 |
| ਚਿੱਤਰ |  |
 |
 |
 |
 |

| |||
| ਸੰਯੋਜਕਤ | ਹਾਈਡ੍ਰੋਜਨ 1 | ਕਰਬਨ 4 ਹਾਈਡ੍ਰੋਜਨ 1 |
ਕਰਬਨ 4 ਹਾਈਡ੍ਰੋਜਨ 1 |
ਕਾਰਬਨ 4 ਹਾਈਡ੍ਰੋਜਨ 1 |
ਨਾਈਟ੍ਰੋਜਨ 3 ਹਾਈਡ੍ਰੋਜਨ 1 |
ਸੋਡੀਅਮ 1 ਕਰਬਨ 4 ਨਾਈਟ੍ਰੋਜਨ 3 |
ਸਲਫਰ 2 ਹਾਈਡ੍ਰੋਜਨ 1 |
ਸਲਫਰ 6 ਆਕਸੀਜਨ 2 ਹਾਈਡ੍ਰੋਜਨ 1 |
ਕਲੋਰੀਨ 7 ਆਕਸੀਜਨ 2 |
ਸਾਂਝੀ ਸੰਯੋਜਕਤਾ
[ਸੋਧੋ]| ਗਰੁਪ | ਸੰਯੋਜਕਤਾ 1 | ਸੰਯੋਜਕਤਾ 2 | ਸੰਯੋਜਕਤਾ 3 | ਸੰਯੋਜਕਤਾ 4 | ਸੰਯੋਜਕਤਾ 5 | ਸੰਯੋਜਕਤਾ 6 | ਸੰਯੋਜਕਤਾ 7 | ਵਿਸ਼ੇਸ਼ ਸੰਯੋਜਕਤਾ |
|---|---|---|---|---|---|---|---|---|
| 1 (I) | NaCl | 1 | ||||||
| 2 (II) | MgCl2 | 2 | ||||||
| 13 (III) | BCl3, AlCl3 Al2O3 |
3 | ||||||
| 14 (IV) | CO | CH4 | 4 | |||||
| 15 (V) | NO | NH3 PH3 As2O3 |
NO2 | N2O5 PCl5 |
3 ਅਤੇ 5 | |||
| 16 (VI) | H2O H2S |
SO2 | SO3 | 2 ਅਤੇ 6 | ||||
| 17 (VII) | HCl | ClO2 | Cl2O7 | 1 ਅਤੇ 7 |
ਹਵਾਲੇ
[ਸੋਧੋ]- ↑ Nakli itihaas jo likheya geya hai kade na vaapriya jo ohna de base te, saade te saada itihaas bna ke ehna ne thop dittiyan. anglo sikh war te ek c te 3-4 jagaha te kiwe chal rahi c ikko war utto saal 1848 jdo angrej sara punjab 1845 ch apne under kar chukke c te oh 1848 ch kihna nal jang ladd rahe c. Script error: The function "citation198.168.27.221 14:54, 13 ਦਸੰਬਰ 2024 (UTC)'"`UNIQ--ref-00000004-QINU`"'</ref>" does not exist.
<ref> tag defined in <references> has no name attribute.